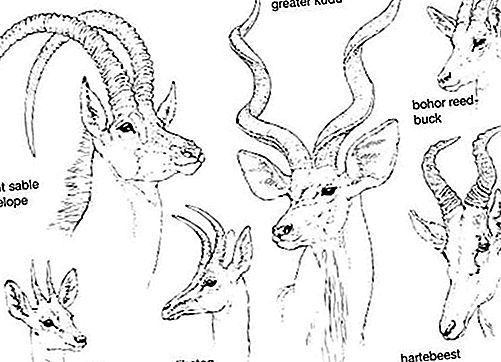
אמפיבול, כל אחד מקבוצה של מינרלים סיליקטיים נפוצים היוצרים סלעים.
שיקולים כלליים
אמפיבולים נמצאים בעיקר בסלעים מטמורפיים וגורמים. הם מופיעים בסלעים מטמורפיים רבים, במיוחד אלה הנגזרים מסלעים מאגיים מאגיים (אלה המכילים מינרלים פרומגנזיים כהים) ודולומיטים סיליקיים. אמפיבולים הם גם מרכיבים חשובים במגוון סלעים פלוטוניים וולקניים, הנעים בהרכבם, גרניטיים וגברוניים. אמפיבול, מהאמפיבולוס היווני, שפירושו "דו משמעי", נקרא על ידי הקריסטוגרף והמינרולוג הצרפתי הנודע רנה-יוסט האוי (1801) ברמיזה למגוון הגדול של ההרכב והמראה שהוצגה על ידי קבוצת המינרלים הזו. ישנן 5 קבוצות עיקריות של אמפיבול המובילות ל 76 קומפוזיציות אמפיבוליות המוגדרות כימית על פי המינרלוג הבריטי ברנרד א. לייק. בגלל המגוון הרחב של תחליפים כימיים המותרים במבנה הגביש, אמפיבולים יכולים להתגבש בסלעים מטוגנים ומטמורפיים עם מגוון רחב של כימיקלים בתפזורת. בדרך כלל אמפיבולים נוצרים כגבישים ארוכים פריזמטיים, תרסיסים מקרינים ואגרגטים אסבסטריים (סיביים); עם זאת, ללא עזרה של ניתוח כימי, קשה לזהות בצורה מסקופית את כל האמפיבולים, פרט לא מעטים, הבולטים יותר. השילוב של צורה פריזמטית ושני כיווני מחשוף בצורת יהלום בערך 56 ° ו- 124 ° הוא המאפיין האבחוני של מרבית חברי קבוצת האמפיבול.
תרכובת כימית
ההרכב הכימי המורכב של חברי קבוצת אמפיבול יכול לבוא לידי ביטוי על ידי הנוסחה הכללית A 0–1 B 2 C 5 T 8 O 22 (OH, F, Cl) 2, כאשר A = Na, K; B = Na, Zn, Li, Ca, Mn, Fe 2+, Mg; C = Mg, Fe 2+, Mn, Al, Fe 3+, Ti, Zn, Cr; ו- T = Si, Al, Ti. החלפה כמעט מלאה עשויה להתקיים בין נתרן לסידן ובין מגנזיום, ברזל ברזלי ומנגן (Mn). קיימת החלפה מוגבלת בין ברזל ברזל לאלומיניום ובין טיטניום לבין קטיונים אחרים מסוג C. אלומיניום יכול להחליף סיליקון בחלקו באתר Tetrahedral (T). תחליף חלקי של פלואור (F), כלור וחמצן להידרוקסיל (OH) באתר ההידרוקסיל נפוץ גם הוא. המורכבות של פורמולת האמפיבול הולידה מספר שמות מינרלים בקבוצת האמפיבול. בשנת 1997 לייק הציגה שמות מדויקים של 76 שמות המקיפים את השונות הכימית בקבוצה זו. השמות המינרליים של האמפיבולים מחולקים לארבע מחלקות עיקריות בהתבסס על תפוסת קטיון בקבוצת B: (1) קבוצת האמפיבול הברזל-מגנזיום-מנגן, (2) הקבוצה האמפיבולה הקאלית, (3) קבוצת האמפיבול הסודי-קלצי, ו- (4) קבוצת אמפיבול סודה. הנוסחאות הכימיות עבור אמפיבולים נבחרים מכל אחת מארבע קבוצות ההרכב ניתנות
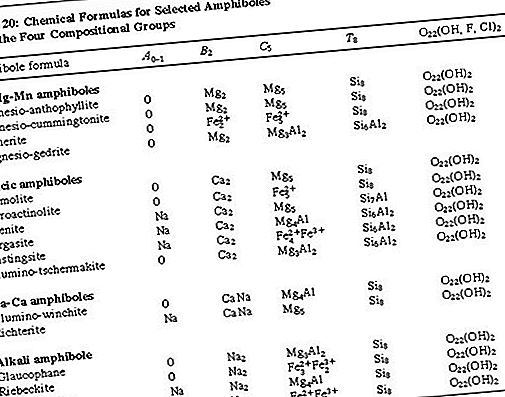
שולחן.
ניתן לייצג מספר רב של אמפיבולים נפוצים בתוך Mg 7 Si 8 O 22 (OH) 2 (מגנוציו-אנתופיליט) –Fe 7 Si 8 O 22 (OH) 2 (גרונריט) - "Ca 7 Si 8 O 22 (OH) 2 " (קומפוזיציה אמפיבולה טהורה בהיפותטית) שדה (איור 1). דיאגרמה זו מכונה בדרך כלל הרביעית האמפיבולה. החלפה מלאה משתרעת מטרמוליט [Ca 2 Mg 5 Si 8 O 22 (OH) 2] לפרו-אקטינוליט [Ca 2 Fe 5 Si 8 O 22 (OH) 2]). אקטינוליט הוא חבר הביניים בסדרת טרמוליט-פארו-אקטינוליט. טווח ההרכבים הוא כ- 0.9 מג"ג 7 Si 8 O 22 (OH) 2 לערך Fe 2 Mg 5 Si 8 O 22 (OH) 2 מיוצג על ידי האמפיבול האורתורומבי המכונה אנתופיליט. הסדרה המונוקוליתית-גרונליט של קאמינגטוניט קיימת בערך Fe 2 Mg 2 Si 8 O 22 (OH) 2 ל- Fe 7 Si 8 O 22 (OH) 2. קומפוזיציות אמפיבול ביניים לא קיימות בין אנתופיליט לסדרה טרמוליט-אקטינוליט. פערים קומפוזיטיביים קיימים גם בין סדרות הקומינגטוניט-גרונריט לבין אמפיבולים קלציים אחרים. כתוצאה מכך, זוגות קיימים של אנתופיליט-טרמוליט וגרונרית-פרואקטינוליט נמצאים יחד בסלעים מסוימים. אמפיבולים נושאי נתרן מיוצגים על ידי הגלוקופאן [Na 2 מג 3 Al 2 Si 8 O 22 (OH) 2] - ריביקיט [Na 2 Fe 2+ / 3 Fe 3+ / 2 Si 8 O 22 (OH) 2]. נתרן נוסף מכיל באתר A במבנה הארפוודסוניט [NaNa 2 Fe 2+ / 4 Fe 3+ Si 8 O 22 (OH) 2]. לאמפיבולים שאינם מאופיינים במדויק בכימיה שלהם, לא ניתן להקצות שם ספציפי. הורנבלנדה הוא השם הכללי המשמש לאמפיבולים קלציים המזוהים רק על ידי תכונות פיסיקליות או אופטיות.
האמפיבולים נבדלים באופן כימי מהפירוקסן בשני היבטים עיקריים. באמפיבולים קבוצות הידרוקסיל במבנה שלהן ונחשבים לסיליקטים הידרוסים היציבים רק בסביבות הידרוזיות בהן ניתן לשלב מים במבנה כ- (OH) -. ההבדל העיקרי השני בהרכב הוא נוכחות אתר A באמפיבולים המכיל את יסודות האלקלי הגדולים, בדרך כלל קטיוני נתרן ולעיתים קטיוני אשלגן. לפירוקסן אין אתר שווה שיכול להכיל אשלגן. נוכחותן של קבוצות הידרוקסיל במבנה אמפיבולים מפחיתה את היציבות התרמית שלהן יחסית לפירוקסן העקשני (עמיד בחום). אמפיבולים מתפרקים למינרלים נטולי מים (בעיקר פירוקסן) בטמפרטורות גבוהות.