Oxyacid, כל חומצה המכיל חמצן. רוב התחמוצות הלא-מתכתיות הקוויליות מגיבות עם מים ליצירת תחמוצות חומציות; כלומר הם מגיבים עם מים ויוצרים חומצות אוקסיד שמניבות יוני הידרוניום (H 3 O +) בתמיסה. ישנם כמה חריגים, כגון פחמן חד חמצני, CO, תחמוצת החנקן, N 2 O ותחמוצת החנקן, NO.
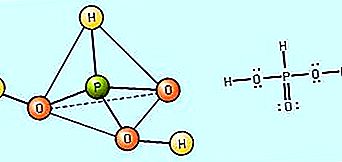
חוזקו של אוקסיד מוגדר על ידי המידה שבה הוא מתנתק במים (כלומר, יכולתו ליצור יוני H +). באופן כללי ניתן לחזות את חוזקם היחסי של חומצות אוקסיד על בסיס מספר האלקטרוני-נגידות וחמצון של האטום הלא-מתכתי המרכזי. חוזק החומצה עולה ככל שהאלקטרוניטיביות של האטום המרכזי עולה. לדוגמא, מכיוון שהמנגנון האלקטרוניטי של הכלור (Cl) גדול מזה של הגופרית (S), שהוא בתורו גדול מזה של הזרחן (P), ניתן לחזות כי חומצה פרכלורית, HClO 4, היא חומצה חזקה יותר מ חומצה גופרתית, H 2 SO 4, שאמורה להיות חומצה חזקה יותר מחומצה זרחתית, H 3 PO 4. עבור אטום מרכזי נתון, חוזק החומצה עולה ככל שמספר החמצון של האטום המרכזי גדל. לדוגמה, חומצה חנקתית, HNO 3, בה אטום החנקן (N) מספר חמצון של +5, היא חומצה חזקה יותר מחומצה חנקנית, HNO 2, בה מצב החמצון של החנקן הוא +3. באותו אופן, חומצה גופרתית, H 2 SO 4, עם גופרית במצב חמצון +6 שלה, היא חומצה חזקה יותר מחומצה גופרתית, H 2 SO 3, בה קיים מספר חמצון של +4 של גופרית.
מלח של חמצן הוא תרכובת הנוצרת כאשר החומצה מגיבה עם בסיס: חומצה + בסיס → מלח + מים. תגובה מסוג זה נקראת נטרול, מכיוון שהפתרון הופך להיות ניטרלי.













