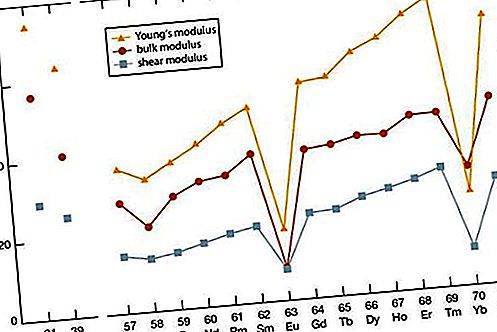
תכונות אלסטיות
כמו ברוב המאפיינים האחרים של מתכות האדמה הנדירות, המודולים האלסטיים של המתכות האדירות הנדירות נופלים באחוזון האמצעי של שאר האלמנטים המתכתיים. הערכים לסקנדיום ויתריום זהים לערך של חברי הקצה של הלנטנידים (ארביום לוטטיום). יש עלייה כללית במודולוס האלסטי עם מספר אטומי הולך וגדל. הערכים האנומליים לסריום (חלקם קשורים ל- 4f) ו- ytterbium (divalency) ניכרים.
תכונות מכאניות
מתכות האדמה הנדירות אינן אלמנטים מתכתיים חלשים ואינם חזקים במיוחד, והם מפגינים מעט משיכות צנועה. מכיוון שהתכונות המכניות תלויות באופן די חזק בטוהר המתכות ובהיסטוריה התרמית שלהן, קשה להשוות בין הערכים המדווחים בספרות. החוזק האולטימטיבי נע בין כ -120 לכ -160 מגה-פיקסל (מגה-סיביות) ומשיכות של בערך 15 עד 35 אחוזים. כוחו של ytterbium (אירופה לא נמדד) קטן בהרבה, 58 מגה-סיביות, והגמישות גבוהה יותר, כ -45 אחוז, כפי שניתן היה לצפות במתכת הדו-שוויאלית.
תכונות כימיות
תגובתיותן של מתכות האדמה הנדירות עם אוויר מציגה הבדל משמעותי בין הלנטנידים הקלים לכבדים. הלנטנידים הקלים מתחמצנים במהירות רבה בהרבה מהלנטנידים הכבדים (גאדוליניום דרך לוטטיום), סקנדיום ויטריום. הבדל זה נובע בחלקו מהשונות של המוצר התחמוצתי שנוצר. Lanthanides האור (לניתן דרך ניאודימיום) מהווה את R A-סוג משושה 2 O 3 מבנה; הלנטנידים האמצעיים (סמריום דרך גאדוליניום) יוצרים את שלב ה- R 2 O 3 המונוקליני; ואילו הלנטנידים הכבדים, הסקנדיום והיתריום יוצרים את שינוי ה- R 2 O 3 מעוקב. סוג ה- A מגיב עם אדי מים באוויר ויוצר אוקסיד-הידרוקסיד, מה שגורם לציפוי הלבן להתפוגג ומאפשר להמשיך לחמצון על ידי חשיפת משטח המתכת הטרייה. התחמוצת מסוג C יוצרת ציפוי הדוק וקוהרנטי המונע חמצון נוסף, בדומה להתנהגות האלומיניום. סמריום וגדוליניום, המהווים את שלב ה- R 2 O 3 מסוג B, מתחמצנים מעט מהר יותר מהלנטנידים הכבדים, הסקנדיום והיתריום, אך עדיין יוצרים ציפוי קוהרנטי שעוצר חמצון נוסף. בגלל זה, יש לאחסן את הלנטנידים הקלים בוואקום או באטמוספירה של גז אינרטי, ואילו ניתן להשאיר את הלנטנידים הכבדים, הסקנדיום והיתריום באוויר הפתוח במשך שנים ללא כל חמצון.
המתכת האירופית, בעלת מבנה bcc, מחמצת את המהירות ביותר מכל אחת מהארצות הנדירות באוויר לח והיא צריכה לטפל בכל עת באטמוספירת גז אינרטי. תוצר התגובה של אירופיום כאשר הוא נחשף לאוויר לח הוא הידרוקסיד הידר, Eu (OH) 2 ―H 2 O, שהוא מוצר תגובה יוצא דופן מכיוון שכל שאר המתכות האדמות הנדירות יוצרים תחמוצת.
המתכות מגיבות במרץ עם כל החומצות למעט חומצה הידרפלואורית (HF), ומשחררות גז H 2 ויוצרות את תרכובת האניון הנדיר-הארץ-נדירה המתאימה. מתכות האדמה הנדירות כאשר מכניסים אותן לחומצה הידרפלואורית יוצרים ציפוי RF 3 בלתי מסיס שמונע כל תגובה נוספת.
מתכות האדמה הנדירות מגיבות בקלות עם גז מימן ליצירת RH 2, ובתנאי הידרידציה חזקים, שלב ה- RH 3 - למעט סקנדיום, שאינו מהווה טריהידריד.
תרכובות
היסודות האדירים הנדירים יוצרים עשרות אלפי תרכובות עם כל היסודות מימין - וכוללים - את מתכות הקבוצה 7 (מנגן, טכנטיום ורניום) בטבלה המחזורית, בתוספת בריליום ומגנזיום, שנמצאים על הרחוק להלן תארים להלן סדרות מורכבות חשובות וכמה תרכובות בודדות עם תכונות ייחודיות או התנהגויות חריגות.
תחמוצות
המשפחה הגדולה ביותר של תרכובות אורגניות נדירות-אדמה שנחקרו עד כה הן תחמוצות. הסטואיציומטריה הנפוצה ביותר היא הרכב R 2 O 3, אך מכיוון שלמרכיבי לנטניד מעטים יש מצבים של ערכים נוספים בנוסף ל -3+, ישנם סטואיציומטריות אחרות - למשל, תחמוצת cerium (CeO 2), תחמוצת פרזודימיום (Pr 6 O 11), תחמוצת טרביום (Tb 4 O 7), תחמוצת אירופה (EuO) ו- Eu 3 O 4. מרבית הדיון יתמקד בתחמוצות הבינאריות, אך גם תחמוצות טרנסיות ואחרות בסדר גבוה יותר ייבדקו בקצרה.