תרכובות אורגניות של גופרית רב-תכליתית: סולפוקסידים וסולפונים
שתי קבוצות עיקריות של תרכובות אורגנו-גופרית שאין להן מקבילים לתרכובות חמצן אורגניות הן הסולפוקסידים והסולפונים. אם ההתאחדות בתרכובות אלה מיוצגת עם מבנים קשורים כפולה - למשל ―S (= O) - לסולפוקסיד ו- ―S (= O) 2 - לסולפון - אטומי הגופרית "רואים" אלקטרונים לערך 10 ו- 12, בהתאמה. זה יותר ממה שכלל האוקטט מאפשר, אך גופרית אינה קשורה לכלל האוקטט, מכיוון שהוא יכול להשתמש באורביטלים תלת-ממדיים במלכודותיו, כפי שיידרש גם בתרכובות כמו hexafluoride גופרית (SF 6). אמנם יש תמיכה תיאורטית מסוימת בהרחבת קליפת הערך הגופרית בכדי להכיל יותר משמונה אלקטרונים, אולם ביקורת על השימוש באורביטלים תלת-ממדיים בתכניות מליטה מכיוון שהאורביטלים התלת-ממדיים הרבה יותר אנרגיה בהשוואה לגופיות 3 ו -3 אורביטלים. מודל מליטה אלטרנטיבי קורא להדבקה קוטבית כמו ―S + (―O -) - לסולפוקסיד ו- ―S 2+ (―O -) 2 - לסולפון. למרות שברור שמבני התהודה הקוטבית תורמים למליטה הכללית, סביר להניח שיש תרומה מסוימת גם מהאורביטלים התלת-מימדיים הגופריים. יש לציין שקבוצת הסולפוקסיד מכילה גם זוג אלקטרונים בודד על אטום הגופרית, המחייב שקבוצת הסולפוקסיד תהיה לא מישורית, דומה לאמין, אך שונה למדי מהמבנה המישורי של קבוצת קרבוניל, ―C (= O) -, שאליה משווים לעתים קבוצת סולפוקסיד. תוצאה חשובה של אי הפלנטריות של קבוצת הסולפוקסיד היא שסולפוקסידים מסוג R (S = O) R where, שבהם R ו- R ′ הם שונים, הם כיראליים ולמעשה ניתן לבודד בצורה פעילה אופטית, עם קבוצת הסולפונים להיות טטרהדרלית. בניגוד לאמינים אך דומים לפוספינים, לגופרית טרי-קואורדינטית (תרכובות גופרית פירמידליות טרימונאליות עם שלושה ליגנדים וזוג אלקטרונים בודד על גופרית - כמו שנמצא למשל בסולפיניל כלורידים, אסטרים גופרתיים, סולפוקסידים, תיוסולפינטים וסולפילימינים) יש תצורה יציבה, בגלל קשרים ארוכים יותר לגופרית (פחות צפיפות) וכמות גדולה יותר של תו זוג בודד (אחוז המסלול בסביבת המספר הכולל של אורביטלים המשמשים בהכלאה). תרכובות טריקורדינטות אקטיביות רבות מופיעות בטבע, ותרכובות גופרית פעילות אופטיות נמצאות בשימוש נרחב בסינתזה של תרכובות כיראליות אחרות.
שמו של הסולפוקסידים נקבע בפשטות, בסדר אלפביתי, של שתי הקבוצות האורגניות המחוברות לקבוצה ―S (= O), ואחריה המילה סולפוקסיד (למשל אתיל מתיל סולפוקסיד, CH 3 S (O) C 2 H 5), או על ידי יצירת קידומת משם הפשוט יותר של הקבוצות המשתמשות בחלקיק- sulfinyl- (למשל, 4- (methylsulfinyl) חומצה בנזואית). המינוח של הגופרת דומה לזה של הגופרית; החלקיקים -סולפוניל משמשים במקרים מורכבים. מרבית הסולפוקסידים הם נוזלים חסרי צבע או מוצקים עם נקודות התכה נמוכות. השפל בעל משקל מולקולרי sulfoxide דימתיל sulfoxide (CH 3 S (= O) CH 3, DMSO) הוא מסיס במים, מציג רעילות נמוכה, והוא ממיס מעולה. יש לו יכולת יוצאת דופן לחדור במהירות לעור ויכול לשאת תרכובות דרך העור בדרך זו. יש לו שימוש מסוים ברפואה וטרינרית, במיוחד בטיפול בזוויות אצל סוסים. סולפונים הם בדרך כלל מוצקים גבישיים חסרי צבע. דימתיל סולפון מסיס במים. השימוש ב- Sulphones Diaryl (pH 2 NC 6 H 4 SO 2 C 6 H 4 NH 2 -p; למשל, דפסון) ותרכובות קשורות לטיפול בשחפת וצרעת. שרפים מפוליסולפון, המשלבים יחידה ―SO 2 C 6 H 4 בתוך פולימר, משמשים בקנה מידה גדול לחלקים חשמליים ורכב ויישומים אחרים הדורשים יציבות תרמית מצוינת ועמידות בפני חמצון.
אירוע והכנה
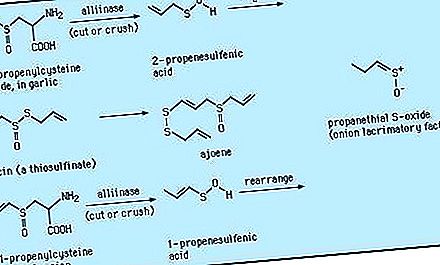
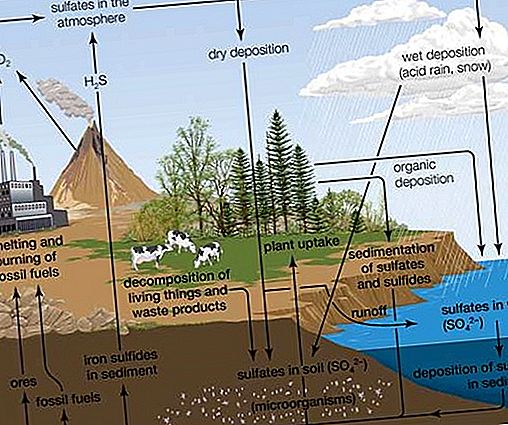
מבין התרכובות שבודדו ממקורות טבעיים, נמצאו הראשונים שיש לטעינה של חומצות S- אלקיל ציסטאין S (כמו S-1- ו- S-2-propenylcysteine S-oxides) - מקדימים את חומרי הטעם של צמחים מהסוג Allium. פעילות אופטית בפחמן כמו גם באלמנט אחר (גופרית). מגוון של sulfoxides אחרים מבודדים מאז ממקורות טבעיים, כולל sulforaphane (CH 3 S (O) (CH 2) 4 NCS) מברוקולי, דיווחו כי הם מעכבים את גידול הגידול, ו- zwiebelanes מתמציות בצל. DMSO נמצא באופן נרחב ברמות של שלושה חלקים למיליון (עמודים לדקה) ומטה והוא מהווה מרכיב נפוץ במים טבעיים, כולל מי ים. יחד עם דימתיל סולפון, DMSO עשוי להיווצר באמצעות מטבוליזם של אצות. כאשר נמצא במי גשמים, DMSO עשוי לנבוע מחמצון של דימתיל סולפיד אטמוספרי, (CH 3) 2 S, המתרחש כחלק מהעברה טבעית של גופרית ממוצא ביולוגי במחזור הגופרית העולמי.
ניתן להכין בקלות את הסולפוקסידים על ידי חמצון של סולפידים עם ריאגנטים כמו metaperiodate נתרן (NaIO 4) או מי חמצן (H 2 O 2). מבחינה מסחרית, DMSO מיוצר מחמצון אוויר / תחמוצת חנקן מזרז של דימתיל סולפיד, שהוא בתורו תוצר לוואי עיקרי של תהליך הסולפט קראפט לייצור נייר. חמצון נמרץ יותר של סולפידים או סולפוקסידים - כמו למשל עם פרמנגנט אשלגן, KMnO 4 - מייצר סולפונים. ניתן להכין סולפוקסידים פעילים באופן אופטי על ידי חמצון סולפידים מסוג RSR where, שם R ≠ R ′, עם חומרים אוקסידיים פעילים או חמצון מיקרוביולוגי. לחלופין, ניתן להכין סולפוקסידים פעילים באופן אופטי באמצעות תגובה של נגזרות סולפיניל פעיל אופטי RS (= O) X, כאשר X = O, N או S, עם ריאגנטים כמו R′Li או R′MgBr. הסולפולין הממיס (תיאולן S, דו-חמצני) מוכן על ידי תגובה ראשונית של דו-תחמוצת הגופרית עם בוטאדיאן כדי לתת סולפולין (סולפון טבעתי מחזור, בלתי-רווי, בעל חמישה חברים), ואחריו מימן למימוש סולפולין.

ניתן לייצר סולפונים ארומטיים גם על ידי תגובה של סולפוניל כלורידים עם פחמימנים ארומטיים. תחמוצות S-Thiophene ו- S, D- דו-תחמוצות, הנוצרות על ידי חמצון של תיואפנים, הן הרבה יותר תגובתי מתיאופנות האביות בגלל אובדן הארומטיות הנובע מהחלפת זוג אלקטרונים אחד או שניהם על גופרית על ידי חמצן.













