קרביד, כל סוג של תרכובות כימיות בהן הפחמן משולב עם אלמנט מתכתי או חצי-מטאלי. סידן קרביד חשוב בעיקר כמקור לאצטילן וכימיקלים אחרים, ואילו הקרבידים של סיליקון, טונגסטן ומספר אלמנטים אחרים מוערכים על קשיותם הגופנית, חוזקם ועמידותם בפני התקפה כימית גם בטמפרטורות גבוהות מאוד. קרביד ברזל (cementite) הוא מרכיב חשוב בפלדה וברזל יצוק.
עיבוד אורניום: דלקים קרביד
ידועים אורניום ופלוטוניום קרבידים שונים, כולל מונוקארבידים (UC, PuC), הססקוויקרבידים (U2C3, .
הכנת קרבידים
קרבידים מוכנים מפחמן ומרכיב בעל אלקטרונטיביות דומה או נמוכה יותר, בדרך כלל מתכת או תחמוצת מתכת, בטמפרטורות של 1,000–2,800 ° C (1,800–5,100 מעלות צלזיוס). כמעט כל קרביד ניתן להכין באחת מכמה שיטות כלליות. השיטה הראשונה כוללת שילוב ישיר של היסודות בטמפרטורות גבוהות (2,000 מעלות צלזיוס ומעלה). השיטה השנייה היא תגובה של תרכובת של מתכת, לרוב תחמוצת, עם פחמן בטמפרטורה גבוהה. שתי שיטות נוספות כוללות תגובה של מתכת או מלח מתכתי עם פחמימן, לרוב אצטילן, C 2 H 2. באחת השיטות המתכת המחוממת מגיבה עם פחמימן גזי; באחרת מתמוססת מתכת באמוניה נוזלית, NH 3, והפחמימן מבעבע בתמיסה. קרבידים המוכנים עם אצטילן נקראים אצטילידים ומכילים את האניון C 2 2. לדוגמה, את אצטיליד המתכות האלקליות מוכנים בצורה הטובה ביותר על ידי המסת המתכת האלקלית באמוניה נוזלית והעברת אצטילן דרך הפתרון. תרכובות אלה, בעלות הנוסחה הכללית M 2 C 2 (כאשר M היא המתכת), הן מוצקות גבישיות חסרות צבע. הם מגיבים באלימות עם מים, כאשר הם מחוממים באוויר, הם מתחמצנים לקרבונט. גם הקרבידות האדמה-אלקלית הם אצטילידים. יש להם את הנוסחה הכללית MC 2 והם מוכנים על ידי חימום המתכת האדמה אלקליין באצטילן מעל 500 מעלות צלזיוס.
סיווג קרבידים
סיווג קרבידים על בסיס סוג מבני הוא די קשה, אך שלוש סיווגים רחבים נובעים ממגמות כלליות בתכונותיהם. המתכות האלקטרופוזיטיביות ביותר יוצרות קרבידים יוניים או מלחיים, מתכות המעבר באמצע הטבלה המחזורית נוטות ליצור מה שמכונה קרבידים בין-עירוניים, והלא-מתכות של אלקטרונגטיביות הדומות לזו של פחמן בצורת קרבידים קוולנטיים או מולקולריים.
קרבידים יוניים
לקרבידים יוניים יש אניוני פחמן נפרדים מהצורות C 4 - המכונים לעיתים מתנידים שכן ניתן לראות בהם כמקורם במתאן (CH 4); C 2 2 - הנקרא אצטילידים ומקורו באצטילן (C 2 H 2); ו- C 3 4 -, נגזר מאלן (C 3 H 4). המתנידים המאופיינים בצורה הטובה ביותר הם ככל הנראה בריליום קרביד (להיות 2 צלזיוס) וקרביד אלומיניום (Al 4 C 3). תחמוצת בריליום (BeO) ופחמן מגיבים בטמפרטורה של 2,000 מעלות צלזיוס (3,600 מעלות צלזיוס) לייצור קרביד הבריליום האדום לבנים, ואילו קרביד אלומיניום צהוב בהיר מוכן מאלומיניום ופחמן בכבשן. קרביד אלומיניום מגיב כמתניד טיפוסי עם מים לייצור מתאן. Al 4 C 3 + 12H 2 O → 4Al (OH) 3 + 3CH 4
ישנם אצטילידים רבים המוכרים ומאופיינים היטב. בנוסף לאלו של המתכות האלקליות ומתכות האדמה-אלקליין שהוזכרו לעיל, לנטנום (La) יוצר שני אצטילידים שונים, ונחושת (Cu), כסף (Ag), וזהב (Au) יוצרים אצטילידים נפיצים. אבץ (Zn), קדמיום (Cd) וכספית (Hg) יוצרים גם אצטילידים, אם כי הם אינם מאופיינים באותה מידה. החשוב ביותר של תרכובות אלה הוא סידן קרביד, CaC 2. השימוש העיקרי בסידן קרביד הוא כמקור לאצטילן לשימוש בתעשייה הכימית. סידן קרביד מסונתז באופן תעשייתי מחמצת סידן (סיד), CaO ופחמן בצורה של קוקה בגובה של כ -2,200 מעלות צלזיוס. נקודת התכה גבוהה של סידן קרביד טהור (2,300 מעלות צלזיוס) והיא מוצקה חסרת צבע. התגובה של CaC 2 עם מים מניבה C 2 H 2 וכמות משמעותית של חום, ולכן התגובה מתבצעת בתנאים מבוקרים בקפידה. CaO + 3C → CaC 2 + CO
CaC 2 + 2H 2 O → C 2 H 2 + Ca (OH) 2 סידן קרביד מגיב גם עם גז חנקן בטמפרטורות גבוהות (1,000–1,200 ° C [1,800–2,200 ° F]) יוצרים ציאנמיד סידן, CaCN 2. CaC 2 + N 2 → CaCN 2 + CT זוהי תגובה תעשייתית חשובה מכיוון ש- CaCN 2 מוצא שימוש נרחב כדשן בגלל תגובתו עם מים לייצור ציאנמיד, H 2 NCN. מרבית האצטילידים של MC 2 הם בעלי מבנה CaC 2, שמקורו במבנה נתרן כלורי (NaCl) מעוקב. יחידות ה- C 2 שוכנות במקביל לאורך צירי התא, וגורמות לעיוות של התא מעוקב לטטרגון.
קרבידות ביניים
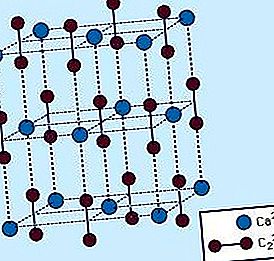
קרבידים בין-עירוניים נגזרים בעיקר ממתכות מעבר גדולות יחסית, המשמשות כסריג מארח לאטומי הפחמן הקטנים, התופסים את הביניים של אטומי המתכת הקרובים. (ראה גביש לדיון על סידורי האריזה במוצקים.) קרבידים ביניים מאופיינים בקשיות קיצונית אך יחד עם זאת שבירות קיצונית. יש להם נקודות התכה גבוהות מאוד (בדרך כלל כ- 3,000–4,000 ° C [5,400–7,200 ° F]) והם שומרים על רבים מהמאפיינים הקשורים למתכת עצמה, כמו מוליכות גבוהה של חום וחשמל וכן ברק מתכתי. בטמפרטורות גבוהות חלק מהקרבידים הביניים שומרים על התכונות המכניות של מתכות, כמו גמישות. לרבות מתכות המעבר המוקדמות יש רדיוסים גדולים מספיק כדי ליצור מונוקארבידים ביניים, MC. הרדיוס הקריטי (כלומר המינימלי) נראה כ- 1.35 אנגסטרם (1.35 × 10 −8 ס"מ, או 5.32 × 10 −9 אינץ '). עם זאת, רוב מתכות המעבר יוצרים קרבידים בין-עירוניים של מספר סטואיציומטריות. לדוגמא, ידוע שמנגן (Mn) יוצר לפחות חמישה קרבידים בין-עירוניים שונים. בניגוד לקרבידים היוניים, מרבית הקרבידים הבין-עירוניים אינם מגיבים עם מים והם אינרטיים מבחינה כימית. לכמה יש חשיבות תעשייתית, כולל טונגסטן קרביד (WC) ו- Tantalum Carbide (TaC), המשמשים ככלי חיתוך במהירות גבוהה בגלל הקשיחות הקיצונית שלהם ואי-הכוח הכימי שלהם. קרביד ברזל (צנטייט), Fe 3 C, הוא מרכיב חשוב בפלדה.