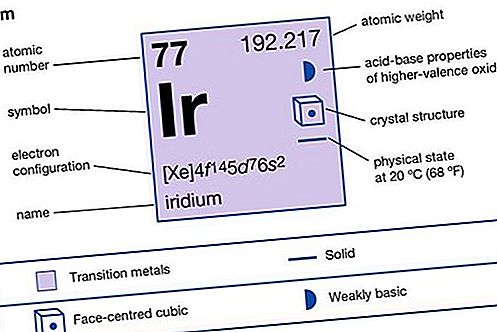
אירידיום (Ir), יסוד כימי, אחת מתכות הפלטינה מקבוצות 8-10 (VIIIb), תקופות 5 ו -6, מהטבלה המחזורית. הוא צפוף מאוד ונדיר ומשמש בסגסוגות פלטינה. אירידיום מתכת יקרה, לבנה כסופה, קשה ושבירה, אך היא הופכת להיות רקיע וניתן לעבוד אותה בחום לבן, בין 1,200 מעלות ל 1,500 מעלות צלזיוס (2,200 מעלות עד 2,700 מעלות צלזיוס). זהו אחד החומרים היבשתיים הצפופים ביותר. במצב מאסיבי המתכת כמעט ולא מסיסה בחומצות ולא מותקפת אפילו על ידי אקווה רג'ה. ניתן להמיס אותו בחומצה הידרוכלורית מרוכזת בנוכחות נתרן פרכלוראט בטמפרטורה של 125 עד 150 מעלות צלזיוס.
בגלל קשיים בהכנה ובייצור, למתכת הטהורה יש מעט יישומים. אירידיום משמש בעיקר בצורה של סגסוגות פלטינה. סגסוגות פלטינום-אירידיום (5 עד 10 אחוז אירידיום) הן מתכות הניתנות לעבודה שהן קשות ונוקשות בהרבה ועמידות יותר בפני התקפה כימית מאשר הפלטינה הטהורה והרכה. סגסוגות כאלה משמשות לתכשיטים, נקודות עט, סיכות כירורגיות וצירים, ומגעים חשמליים ונקודות ניצוץ. קילוגרם המסה הסטנדרטי של אב הטיפוס הבינלאומי עשוי מסגסוגת המכילה 90 אחוז פלטינה ו -10 אחוז אירידיום.
אירידיום טהור כנראה לא מתרחש בטבע; השפע שלו בקרום כדור הארץ הוא נמוך מאוד, כ- 0.001 חלקים למיליון. אם כי נדיר, אירידיום מופיע בסגסוגות טבעיות עם מתכות אצילות אחרות: באירידממין עד 77 אחוז אירידיום, בפלטינירידיום עד 77 אחוז, באורוסמירידיום 52 אחוז, ובפלטינה ילידית עד 7.5 אחוז. אירידיום בדרך כלל מיוצר באופן מסחרי יחד עם מתכות הפלטינה האחרות כתוצר לוואי של ייצור ניקל או נחושת.
עפרות המכילות אירידיום נמצאות בדרום אפריקה ובאלסקה, ארה"ב, כמו גם במיאנמר (בורמה), ברזיל, רוסיה ואוסטרליה. בסוף המאה העשרים הייתה דרום אפריקה המייצרת העיקרית בעולם של אירידיום.
היסוד התגלה בשנת 1803 בשקעים הבלתי-מסיסים של עפרות פלטינה על ידי הכימאי האנגלי סמיתסון טננט; הכימאים הצרפתים H.-V. קולט-דקוטילים, A.-F. פורקרוי, ונ.ל. ווקלין זיהה את זה בערך באותה עת. השם אירידיום, שמקורו במילה היוונית איריס ("קשת בענן"), מתייחס לצבעים השונים של תרכובותיו. אירידיום טבעי מורכב מתערובת של שני איזוטופים יציבים, אירידיום -191 (37.3 אחוז) ואירידיום -193 (62.7 אחוז). הכימיה של אירידיום מתרכזת במצבי חמצון של +1, +3 ו- +4, אם כי תרכובות של כל המצבים בין 0 ל- +6 ידועות למעט +2. מתחמים במצב חמצון +1 מכילים בעיקר פחמן חד-חמצני, אולפינים ופוספינים כליגנדים. האניונים hexachloroiridate, [IrCl 6] 2−, ו- hexabromoiridate, [IrBr 6] 2−, הם המינים הכימיים הבולטים היחידים המכילים אירידיום במצב החמצון +4. אירידיום הוא תגובתי מעט יותר מאשר רותניום ואוסמיום.
מאפייני אלמנט
| מספר אטומי | 77 |
|---|---|
| משקל אטומי | 192.2 |
| נקודת המסה | 2,410 מעלות צלזיוס |
| נקודת רתיחה | 4,527 ° C (8,181 ° F) |
| כוח משיכה ספציפי | 22.4 (20 מעלות צלזיוס) |
| מצבי חמצון | +1, +3, +4 |
| תצורת אלקטרונים. | [Xe] 4f 14 5d 9 |